Prawidłowo korozję nazywa się korozją elektrochemiczną, na skutek korozji następuje niszczenie powierzchni metalu podczas zachodzących reakcji elektrochemicznych. Dobre zrozumienie procesu powstawania korozji pozwala na lepsze dobranie środków antykorozyjnych i ochrony chemicznej oraz skuteczną ochronę przed skutkami korozji.
Zazwyczaj korozja elektrochemiczna powstaje na zetknięciu się dwóch metali i uwarunkowaniem dla jej powstania są drobne wtręty obcego metalu. Co przyczynia się do powstania trwałego ogniwa galwanicznego, w którym elektrolitem jest skroplona para wodna z powietrza. W której to rozpuszcza się pochodzący z powietrza ditlenek węgla(CO2), tworząc kwas węglowy. Jak również pochodzący z gazów spalinowych ditlenek siarki (SO2), po rozpuszczeniu się w skroplonej parze wodnej tworzy kwas siarkowy (IV).
SO2 + H2O → 2 H+ + SO32-
Podczas zetknięcia się metale wraz z elektrolitem tworzą ze sobą ogniwo korozyjne, które możemy traktować jako ogniwo galwaniczne.
Podczas zachodzących reakcji elektrochemicznych zachodzą dwa procesy :
- Proces anodowy, podczas którego następuje utlenienie metalu nieszlachetnego.
M → M z+ + ze
- Proces katodowy, natomiast zachodzi redukcja tlenu, wówczas nazywamy to korozją tlenową
½ O2 + H2O + 2e → 2OH-
Jeżeli w procesie katodowym następuje redukcja jonów wodorowych
2 H+ + 2e → H2
taki proces, nazwiemy korozją wodorową.
 Powstanie korozji tlenowej, jest możliwe w roztworach obojętnych lub alkaicznych, a korozja wodorowa zachodzi w roztworach kwaśnych, dla pH mniejszego od 4.
Powstanie korozji tlenowej, jest możliwe w roztworach obojętnych lub alkaicznych, a korozja wodorowa zachodzi w roztworach kwaśnych, dla pH mniejszego od 4.
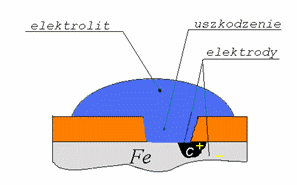
jeżeli na styku żela i innego metalu znajdzie się kropla wody, w której zawarty jest tlen z powietrza, zachodzą procesy elektrochemiczne. Podczas których następuje utlenienie żelaza do jonów żelaza Fe2+, które przechodzą do roztworu. Elektrony e pochodzące od żelaza przechodzą do drugiego metalu, przyczyniając się do redukcji tlenu do jonów wodorotlenowych OH-. Co przyczynia się do powstania wodorotlenku żelaza (II) Fe(OH)2 , który pod wpływem wody i powietrza tworzy rdzę, zawierającą między innymi FeO(OH).
Fe + ½ O2 + H2O → Fe2+ + 2OH-
Ogniwa galwaniczne, także powstają również, kiedy nie ma styku dwóch różnych metali , zależne jest wówczas różnych stężeń jonów tego samego metalu. Taką korozję nazywamy korozją stężeniową.
Dlatego każdy użytkownik samochodu powinien zawsze pamiętać o odpowiednim zabezpieczeniu swojego auta przed niedopuszczeniem do osadzania się na elementach metalowych nadwozia jak i podwozia pary wodnej. Przy systematycznej antykorozyjnej konserwacji przestrzeni zamkniętych nadwozia okres użytkowania samochodu-jak wskazują badania – wydłuża się dwukrotnie. Skuteczne przedłużenie żywotności auta, zapewnia regularne stosowanie preparatów antykorozyjnych o specjalnych właściwościach sprawdzonych w praktyce na wielu pojazdach w czasie wieloletnich badań eksploatacyjnych, jak między innymi FLUIDOL MLP.
Korozję elektrochemiczną też możemy ograniczać, poprzez zabezpieczanie elementów metalowych, poprzez nałożenie lakieru bądź stosując skuteczne powłoki metaliczne zapewniające długą ochronę przed korozją. Powłoka metaliczna nakładana na metal, wykorzystuje zjawisko pasywacji, czyli na powierzchni ochronnej tworzą się tlenki metali(chromu, niklu glinu). Do tego celu możemy wykorzystać dostępne już na rynku preparaty metli w sprayu jak np.. Aluminium-Spray A-100.
Zobacz pełną bazę produktów: preparaty antykorozyjne do stali.
Korozja to proces degradacji metali będący wynikiem reakcji elektrochemicznych z otoczeniem (np. wodą, tlenem, substancjami chemicznymi). Zjawisko korozji elektrochemicznej to nie tylko obniża wytrzymałość konstrukcji, ale także generuje koszty konserwacji i napraw. Dlatego ważne jest stosowanie metod ochronnych, które spowalniają lub całkowicie hamują przebieg tego procesu.
więcej »










